Zapisy
W 2022 ROKU KURSY Z DR N. MED. WOJCIECHEM RYBAKIEM ZOSTAŁY WSTRZYMANE.
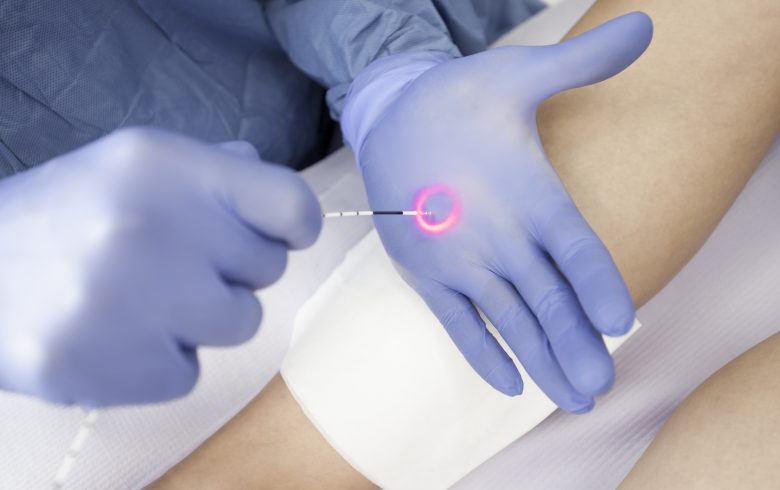
Kurs laseroterapii wewnątrzżylnej I stopnia
Zapraszamy do udziału w indywidualnym kursie laseroterapii wewnątrzżylnej na poziomie podstawowym, który realizowany jest przez dr n. med. Wojciecha Rybaka – wieloletniego praktyka z zakresu leczenia przewlekłej niewydolności żylnej oraz flebologii estetycznej. Kurs obejmuje szeroki zakres wiedzy teoretycznej omawiającej problematykę niewydolności żylnej oraz część praktyczną skoncentrowaną na doskonaleniu umiejętności zabiegowej. Szkolenie zaprojektowane jest w taki sposób, by uczestnik miał możliwość samodzielnego przeprowadzenia zabiegów o różnym stopniu zaawansowania.
Kto może przystąpić do szkolenia
Zarówno podstawowy jak i zaawansowany poziom szkolenia z laserowego leczenia niewydolności żylnej dedykowany jest praktykującym lekarzom o specjalizacji zabiegowej.
Program kursu
W trakcie tworzenia.
Koszt uczestnictwa
Ostateczna cena szkolenie indywidualnego z zakresu leczenia niewydolności żylnej za pomocą lasera wewnątrznaczyniowego na poziomie podstawowym zostanie ustalona po stworzeniu programu kursu.
Informacje dodatkowe
Dwudniowy kurs zakończony jest egzaminem teoretycznym i praktycznym. Warunkiem otrzymania certyfikatu jest uzyskanie pozytywnej oceny z obu części egzaminu.
Warunkiem uczestnictwa w szkoleniu zaawansowanym jest odbycie kursu na poziomie podstawowym.